Новое исследование, проведённое в Иллинойском университете в Чикаго, выявляет важную связь между состоянием кровеносных сосудов в мышцах и возникновением мышечной слабости и потери веса у людей с раковыми заболеваниями. Открытие даёт надежду на разработку инновационных подходов для восстановления мышечной силы и улучшения качества жизни пациентов после лечения.
Кахексия: основная угроза для онкологических пациентов
Кахексия — это истощающее состояние, сопровождающееся быстрой потерей мышечной массы, снижением веса и постоянной усталостью, которое испытывает до 80% больных с онкологией. Оно резко снижает физические возможности, затрудняет повседневную активность и существенно влияет на исход лечения. Несмотря на распространённость этой проблемы, эффективных стратегий для её предотвращения и обращения ещё не найдено.
Роль кровеносных сосудов в развитии мышечной атрофии
Мышечные кровеносные сосуды не только снабжают ткани питательными веществами и кислородом, но и активно участвуют в поддержании работы органов и тканей. При прогрессировании ракового процесса специфические молекулы, вырабатываемые опухолью, способны запускать цепь изменений в структуре и функции сосудов, что приводит к их нарушенной деятельности и ухудшению состояния мышц.
Научная группа Иллинойского университета выделила, что уничтожение или деградация сосудистой структуры негативно отражается на обмене веществ, вызывает гибель мышечных волокон и снижает силу, делая невозможной полноценную реабилитацию пациентов после онкологических заболеваний.
Прорыв в анализе причин кахексии
Традиционно учёные фокусировались на воспалительных процессах, которые происходят под действием нарушенного иммунного ответа у больных с кахексией. Считалось, что мышечная атрофия напрямую связана с атакой иммунных клеток на ткань. Однако новое направление исследований позволило выявить, что ключевую роль играет именно сосудистый компонент: изменение свойств эндотелиальных клеток, выстилающих внутреннюю поверхность сосудов, запускает цепные реакции, приводящие к истощению мышечной массы.
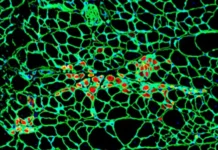
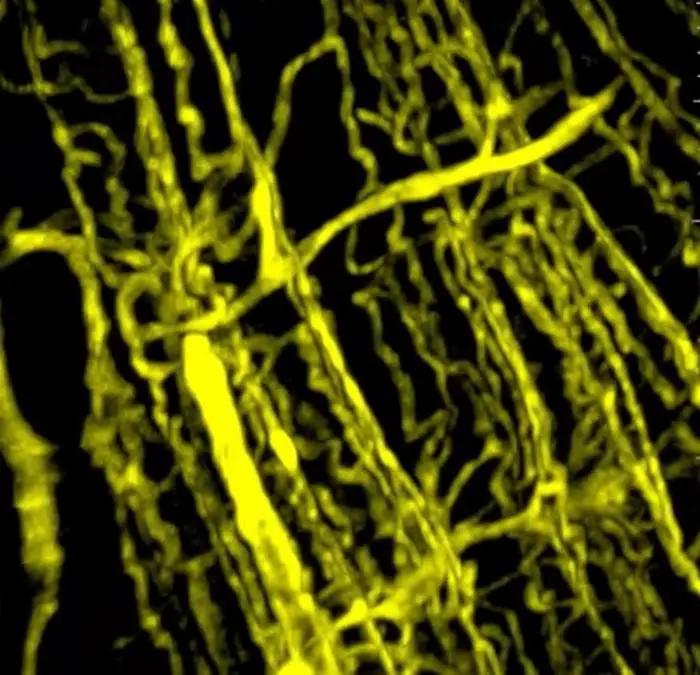
В ходе анализа различных моделей рака, в том числе образцов тканей человека и животных, учёные обнаружили явное уменьшение количества и толщины сосудов. Это подтверждается результатами современных 3D-микроскопических исследований: больные мышцы отличаются меньшей васкуляризацией и худшими показателями прочности по сравнению со здоровыми.
Ключ к восстановлению: активин А и белок PGC1α
Особое внимание специалистов привлекла молекула активин А, которая в избыточных количествах накапливается в эндотелиальных клетках при наличии у пациента онкологического процесса. Она играет роль «тормоза», снижая экспрессию белка PGC1α – важного регулятора энергетического обмена и восстановления сосудистой сети. Этот белок отвечает за формирование новых сосудов, поддержание их целостности и жизнеспособности мышц.
Экспериментальное повышение активности PGC1α в мышечных сосудах позволило вернуть им здоровье, улучшить кровообращение и, как следствие, восстановить работоспособность самой мышцы даже на фоне сильного заболевания. Таким образом, мишени для будущих лекарственных препаратов обозначились чётко: необходимо либо снижать уровень активина А, либо усиливать экспрессию PGC1α. Это открытие формирует фундамент для разработки новых подходов к терапии кахексии у онкологических больных.
Оптимистичный взгляд в будущее
Работа учёных Иллинойского университета в Чикаго открывает реальные перспективы помочь миллионам людей по всему миру, страдающим от тяжёлых последствий онкологических заболеваний. Восстановление сосудистого русла мышц благодаря целевому воздействию на активин А и PGC1α становится одной из самых перспективных областей современной онкологии и реабилитационной медицины.
Команды экспертов уже работают над созданием лекарственных средств и методик, способных запускать процессы регенерации мышц у тех, кто прошёл тяжёлый путь борьбы с раком. Инновационные исследования дают надежду вернуть активность, самостоятельность и качество жизни, способствуя быстрому восстановлению после лечения.
Заключение
Развитие технологий в сфере молекулярной биологии и генетики позволяет глубже изучать механизмы развития кахексии и разрабатывать персонализированные схемы лечения для пациентов с раком. Усиление регенерации мышц и поддержание здоровья сосудов с помощью воздействия на активин А и PGC1α — это новое слово в медицине, обещающее эффективную защиту от мышечной атрофии. Эти исследования служат вдохновляющим примером научного прогресса и дают реальный шанс на качественное восстановление жизни после тяжёлых испытаний.